CRISPR/Cas9で糖尿病に立ち向かう!? ~ゲノム編集技術を用いたCommon diseasesの研究-②~

コロナ禍における生活習慣の変化
2019年に中国武漢で感染拡大が発覚し、瞬く間に世界中に広がったCOVID-19。これにより、我々の生活はそれ以前と全く違ったものに変わってしまった。街ゆく人々は皆マスクを付け、ありとあらゆる場所で飛沫対策のセパレートや消毒が設置されるようになった。特に飲食店においては、緊急事態宣言の発令に伴って営業休止や時間短縮、酒類提供の停止などのさまざまな措置が執られ、大人数での食事会や仕事終わりの居酒屋での飲み会は街からすっかり姿を消してしまった。これを読んでいる方々も、家の外でお酒を飲む機会は激減した方がほとんどだろう。
しかし、その一方で、自宅で過ごす時間が増えたことで飲酒量が増加した方も多いのではないだろうか。今年の4月にキリンホールディングス株式会社が発表したアンケート[1]によれば、コロナ禍になりほとんどの人が自宅外での飲酒機会は減ったにも関わらず、トータルの飲酒量では6割ほどの人は以前と変わらず、3割ほどの人に至っては逆に増えたと回答したという。これには、自宅生活が長引いたことによって自宅での飲酒量が増えたり、テレワークにより仕事とプライベートの区別がつきにくくなってストレスの解消先を飲酒に向けてしまったりと様々な理由が考えられるだろう。こうしたトータルの飲酒量の増加は、コロナ禍の影響が多方面かつ長期的に現れていることがよく分かる一例だ。
そのほかにもオンライン化に伴って通勤・通学がなくなったことで運動時間や日光を浴びる時間が短くなったり、一人暮らしの方はコンビニ食が増えたりと、コロナ禍で生活習慣が乱れる要因はたくさんあっただろう。(もちろんコロナ禍で逆に生活習慣が改善するように作用したポイントもあるので一概に悪いとは言えないが)。
そして、こうした生活習慣の乱れは、前回の著者の記事[2] でも触れたように肥満症や糖尿病などの生活習慣病と呼ばれる疾患の原因となり得る。例えば、多量の飲酒は糖尿病のリスクを増加すると言われている[3]。アルコールを摂取すると、アルコールそのもの作用やアルコールの代謝によって血糖値は変化する。適度な飲酒は糖尿病の発症を抑制する一方で、多量の飲酒は糖尿病の発症を促進する可能性があるといくつかの臨床試験で報告されている[4-5]。
そこで今回は前回の肥満症に引き続き、頻度が高くかつゲノム編集技術による治療が検討されている糖尿病を扱っていく。2つの記事を通して我々の健康で文化的な生活を維持するためのヒントを得ていただければ幸いである。
糖尿病とその疫学
そもそも糖尿病とは、血糖値を下げるホルモンであるインスリンの作用不足によって高血糖が慢性的に続く病気のことである[6]。血糖値とは主に血中のグルコース濃度のことを指す。血糖値を調節するインスリンは、通常血糖値の上昇に伴い膵臓のランゲルハンス島にあるβ細胞から分泌され、細胞膜のインスリン受容体に結合することで肝臓や脂肪細胞、骨格筋細胞へのグルコースの取り込みを促進する[7]。
糖尿病によって血糖値が上昇すると血管障害が生じる。微小な血管障害では網膜症、腎障害、神経障害の三大合併症、中血管や大血管障害では心筋梗塞や脳梗塞、閉塞性動脈硬化症などのさまざまな合併症を発症することが知られている[8]。
糖尿病の診断はやや複雑であり、日本糖尿病学会の「糖尿病治療ガイド2020-2021」では以下のような糖尿病フローでは提唱されている [9]。
〜糖尿病の診断〜
まず、以下の4つの値を計測する。
①ヘモグロビンA1c(HbA1c)
ヘモグロビンを構成するβ鎖のN末端にグルコースが結合したタンパク質のことであり、過去1~2ヵ月間の平均の血糖状態を示すとされている。
②早朝空腹時血糖値
8時間以上の絶食後である早朝に採血した際の血糖値である。
これは75gのブドウ糖を経口で摂取し、その2時間後に測定した血糖値である。
④随時血糖値
これは食事時間によらず採血した際の血糖値である。
そして、このそれぞれの値について、
(1)早朝空腹時血糖値が126mg/dL以上
(2)75gOGTTが200mg/dL以上
(3)随時血糖値が200mg/dL以上
(4) HbA1cが6.5%以上
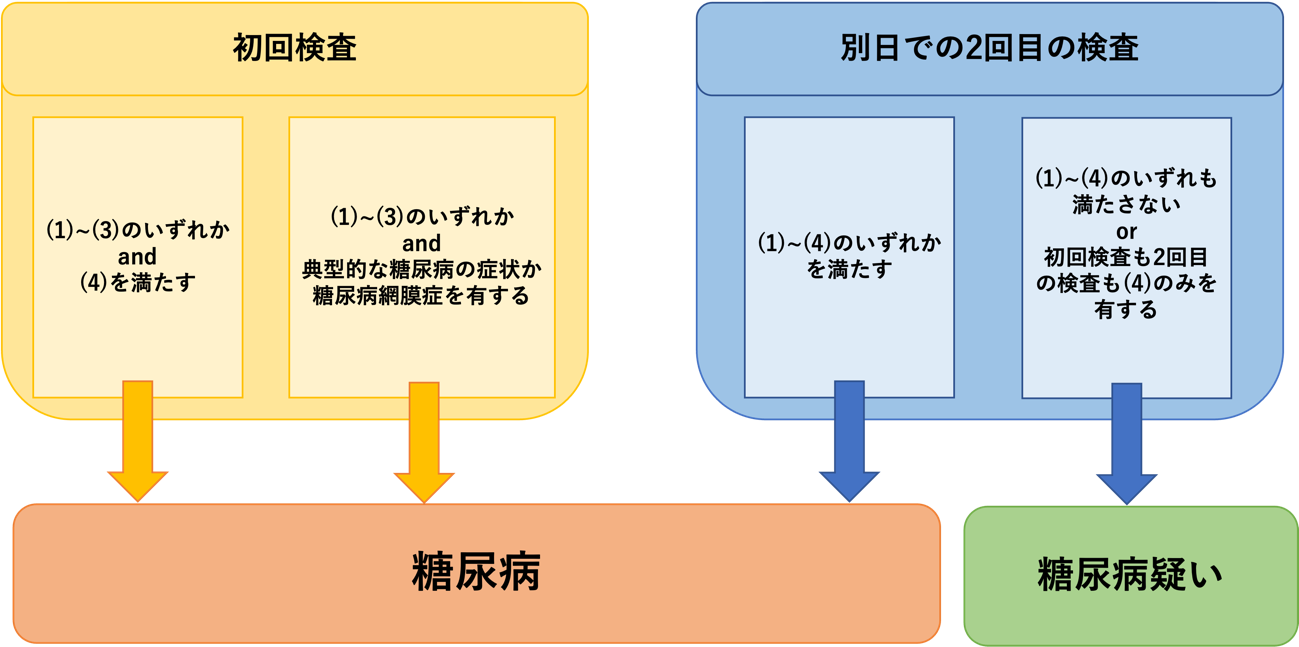
の4つの基準があり、まずこのうち1つでも満たせば糖尿病型と診断される。そして以下のフローにより糖尿病が診断される(図1)。なお、初回検査で糖尿病型であって糖尿病の診断に至らなかった場合に別日での2回目の検査を行う。
また、糖尿病は病態生理によって主に次の3つのサブタイプに分けることが出来る。
①1型糖尿病
遺伝的素因によりβ細胞に対する自己抗体が作られてβ細胞が破壊された結果、インスリンの産生が低下するタイプ。生活習慣の改善によって病態が改善するわけではなく、多くは若年発症であり、患者は早期からインスリンの自己注射を必要とする。
②2型糖尿病
遺伝的素因だけではなく、環境的素因としての生活習慣の悪化を原因とする糖尿病。インスリン抵抗性(インスリンの効き目が悪くなる)によりインスリンが相対的に不足したり、その結果膵臓のβ細胞が分泌能を失ったりする。このタイプが最も多い。
③妊娠中の糖尿病
妊娠中はインスリンの分泌および抵抗性によって血糖値が上昇しやすいといわれている。そのため、糖代謝異常を引き起こしやすく、発症及び診断に至ったタイミングなどによって「妊娠糖尿病」、「妊娠中の明らかな糖尿病」、「糖尿病合併妊娠」の3つに分類されている[10]。
そして厚生労働省が実施した令和元年国民健康・栄養調査[11]による糖尿病が強く疑われる人口の割合は次のようになった(表1)。
(表1)令和元年における日本の成人の糖尿病が強く疑われる人口の割合 (%)
| 20-29歳 | 30-39歳 | 40-49歳 | 50-59歳 | 60-69歳 | 70歳以上 | 全年代 | |
|---|---|---|---|---|---|---|---|
| 男性 | 0 | 1.6 | 6.1 | 17.8 | 25.3 | 26.4 | 19.7 |
| 女性 | 0 | 2.6 | 2.8 | 5.9 | 10.7 | 19.6 | 10.8 |
前回紹介した肥満症よりも割合こそ低いものの、高齢男性では4人に1人、高齢女性でも5,6人に1人は糖尿病が強く疑われており、日本全体で見れば相当な数の患者がいることが予想される。
現状の糖尿病の治療
糖尿病の治療と聞くと何を思い浮かべるだろうか? おそらくインスリンの自己注射や人工透析と答える方が多いだろう。これを読んでいる方やそのご家族にもインスリンの自己注射をされている方がいたり、住む街の近くに透析クリニックがあったりすると、このように考えるのも自然だろう。
しかし、肥満症と同様に、実際の糖尿病の治療はかなり複雑で、多くの問題点を抱えている。ここでは主に罹患者の多い2型糖尿病に注目して見ていこう。
まず、2型糖尿病の治療の基本は食事療法と運動療法である。患者は糖尿病の原因となり得る不適切な食生活を正し、運動療法により過剰なエネルギーを消費したり、筋肉の活動量が上げ、インスリンの抵抗性を改善したりすることを目的とする。
これでも改善が見られない患者は、薬物療法を検討する。もっともメジャーなものはインスリン注射である。インスリンは血糖値を下げるホルモンそのものであるが、自己注射をする必要があるために侵襲性が高い。また、次第にインスリンは効き目が悪くなるために投与量が増加していくことが多い。これは長期的に付き合う必要のある糖尿病の治療としては必ずしも良い選択とは限らないだろう。
そこでインスリンがなくとも生命維持には影響しないと考えられる患者には、その他の薬剤を導入する。現状日本で承認されている治療薬には以下のようなものがある。(表2)
(表2)主な糖尿病治療薬
| 薬剤分類 | 薬剤の例 | 作用機序 | 副作用の例 |
|---|---|---|---|
| ①インスリン抵抗性改善薬 | |||
| ビグアナイド系 | Metformin | ミトコンドリア内膜のmGPDの抑制による肝臓での糖新生とグルカゴンの作用を抑制する。
解糖系や末梢のグルコースの取り込みを促進する。 |
Lacticアシドーシス、Vitamin B12欠乏 |
| チアゾリジン系 | Pioglitazone, Rosiglitazone | PPAR-γを活性化してインスリンの感受性やadiponectinの活性を高めてグルコースや脂質の代謝をコントロールする。 | 心不全、浮腫
骨折リスク、体重増加 |
| ②インスリン分泌量増加 | |||
| 第1世代 スルホニルウレア系 | Chlorpropamide, Tolbutamide | 膵臓のβ細胞のK+チャネルを閉じて脱分極させ、カルシウム依存性のインスリン放出を促進する。 | 低血糖 |
| 第2世代 スルホニルウレア系 | Glipizide, glyburide | ||
| Meglitinides系 | Nateglinide, Repaglinide | ||
| ③グルコース依存性インスリン分泌促進 | |||
| GLP-1 analog | Exenatide, liraglutide | グルカゴンの作用を低減させてグルコース依存性のインスリン放出を誘導する。 | 嘔気、膵炎、過度な体重減少 |
| DPP-4阻害薬 | Linagliptin, Saxagliptin, Sitagliptin | GLP-1を抑制するDPP-4を阻害することでグルコース依存性のインスリン放出を誘導する。 | 自己免疫疾患・皮膚障害 |
| ④グルコースの吸収量低下 | |||
| SGLT-2阻害薬 | Canagliflozin, Dapagliflozin, Empagliflozin | 近位尿細管におけるグルコースの再吸収量を減らす。脂肪の燃焼効率を高める。 | 脱水、減量、尿路感染症 |
| α-glucosidase 阻害薬 | Acarbose, miglitol | 小腸冊子縁の糖質の加水分解とグルコースの吸収を遅延させ、食後の高血糖を抑制する。 | 下痢・便秘・腹部膨満 |
| ⑥その他 | |||
| グリミン系 | Imeglimin | 2021年6月に承認された。ミトコンドリアの呼吸鎖複合体に作用し、膵臓のβ細胞の保護作用に加えて、肝臓、筋肉におけるインスリンの作用を増強する。 | 臨床試験中 |
以上に挙げたように、既に多くの糖尿病治療薬が承認されている。特に今年(2021年)の6月には、これまでの作用機序とは全く異なる新規治療薬(ファーストインクラスと呼ばれる)として期待されるImegliminが新たに承認された[12]。これはこれまでの糖尿病の薬剤よりも、病気の原因となっている部分によりアプローチしようとする薬剤である。近年病態解明が進むにつれてさまざまな疾患の治療薬においてこのような傾向が見られる。今後もこのような薬剤開発が進んでいくだろう。
しかし、このImegliminでさえも、治療効果が乏しい患者は一定数出てくるだろう。糖尿病のメカニズムが完全に理解されているわけではない以上は、開発された薬剤が根治につながるという因果関係までは言うことができないし、薬剤が患者集団の多くに効果が見られることと、どの患者にでも効果が見られるというのは必ずしもイコールではないからだ。そこで今回は、糖尿病の病態解明および治療について行われている研究のうち、ゲノム編集の側面からアプローチしている研究を取り上げていこう。
ゲノム編集技術について
まず、簡単にゲノム編集について説明し、中でも現代のゲノム編集の主要技術となっているCIRSPR/Cas9について紹介しよう。ゲノム編集技術とは、生物を構成する細胞の遺伝情報であるゲノムを人為的に編集することで目的の形質や性質を生物に獲得させるというものである。CRISPR/Cas9はその技術の中でも、第三世代のゲノム編集技術と呼ばれ、現在のゲノム編集の中心技術となっている。
CRISPR/Cas9の仕組みは、標的のDNA配列を、tracrRNAと複合させたガイドRNAとcrRNA、さらにCas9と呼ばれるハサミの役割を持つ物質と一緒に導入することで、その配列を特異的に切断し、目的の遺伝子をノックアウトさせたり、DNA切断に伴う修復機構を利用し、逆に外部からドナーDNA を導入することで目的の遺伝子をノックインさせたりすることもできるという技術である。近年では野菜や植物の編集、遺伝子疾患など様々な領域において利用されている。(CRISPR/Cas9についての詳細はセツロテックMEDIAに掲載の筆者執筆の記事を参考にされたい[13])。
糖尿病に対するゲノム編集治療の研究
ここからは主に、CRISPR/Cas9を用いたゲノム編集による糖尿病の研究をいくつか紹介していきたい。
①糖尿病のマウスモデルについて
まずは2018年、Roh氏らによって発表された研究を紹介しよう[14]。彼らによれば、糖尿病の遺伝子座(染色体上の遺伝子が存在する固有の位置)はよく研究が進んでおり、1994年にレプチン(Lep)、1996年にレプチン受容体(Lepr)がそのうちの正体の1つとして同定されていた。レプチンは主に白色脂肪組織(WAT)で産生されるアミノ酸のペプチドであり、体内の各組織にあるレプチン受容体と結合してエネルギーバランスの調節や体重のコントロールに重要な役割を果たしている。また、それだけではなく、脳の視床下部にもレプチン受容体が存在し、この受容体を介して、満腹中枢における食欲のコントロールに寄与している。マウスレベルでは、レプチンおよびその受容体遺伝子の変異によって、早期からの肥満とそれに伴うインスリン抵抗性を伴う高血糖、糖尿病が起こることが報告されている。
そこでRoh氏らは、CRISPR/Cas9によって効率よくレプチンおよびその受容体をノックアウトしたモデルマウスを作成することに成功した。そしてこのマウスを12時間ごとに明暗の逆転する箱の中で昼夜を一定リズムに保ちながら普通の餌を与えて飼育し、血糖値、インスリン濃度などを測定した。
その結果、レプチン遺伝子を欠損させたモデルマウスでは、肥満が顕在化する前に高血糖が観測された。空腹時の血糖値と血中インスリン濃度も上昇し、インスリン抵抗性の指標であるHOMA-IRが上昇したマウスの存在も確認された。また、レプチン受容体遺伝子を欠損させたモデルマウスにおいても、HOMA-IR指標の顕著な上昇が検出され、高血糖、著しい耐糖能低下、インスリン抵抗性を伴うことが示された。
この研究は、全身性疾患である糖尿病においても、CRISPR/Cas9がその研究に応用可能であることが示唆された貴重な研究であると言えるだろう。
②ヒト幹細胞由来のβ細胞の作成による糖尿病治療の検討
次はiPS細胞でおなじみのヒト幹細胞をCRISPR/Cas9で編集し、膵臓のβ細胞機能をもった細胞を作成した研究を紹介する。この研究は2020年にMaxwell氏らによってSci Transl Medに公表されたものである[15]。これまで、いくつもの研究で糖尿病患者由来のiPS細胞から膵臓のβ細胞を作成する試みがなされてきた。しかし、いずれも失敗率が高く、また十分な生理機能を持たないことが問題視されてきた。
そこでMaxwell氏らは、糖尿病を起こす様々な疾患のうち、WFS1遺伝子という遺伝子の変異によって糖尿病症状を引き起こすWolfram Syndromeという遺伝性疾患に注目した。Wolfram Syndromeは細胞内の小胞体という構造物に慢性的なストレス(小胞体ストレス)を引き起こし、最終的にはβ細胞の死を引き起こすことで小児期から糖尿病を発症させることが知られている。
彼らは、このWS患者の皮膚の線維芽細胞からiPS細胞を作成し、さらにCRISPR/Cas9によってWFS1遺伝子を編集してβ細胞に分化させた。そしてこのβ細胞を糖尿病のモデルマウスに移植した。その結果、このモデルマウスはインスリンの分泌がおこり、平均血糖値が80mg/dLほどまで低下したという。
この研究は、糖尿病を誘発する遺伝子変異をCRISPR/Cas9で修復することで、正常な機能を持つβ細胞を作成し、糖尿病を治療できる可能性を示唆する研究となった。
③複数のDNA配列を対象としたβ細胞のゲノム編集研究
最後に紹介するのは、2021年にBevacqua氏らによってNature communicationsに投稿された研究である[16]。この研究では、ヒト膵臓のβ細胞そのものの遺伝子を編集し、各遺伝子の発現とβ細胞の機能の変化について研究した。彼らはβ細胞のDNA配列のうち、エンハンサー(遺伝子発現を促進する配列部分)をターゲットにしてCRISPR/Cas9による編集を行った。その結果、ABCC8、SIX2、SIX3などの遺伝子の発現が低下し、β細胞のインスリン分泌機能が低下したことがわかった。この研究は、糖尿病の直接的な原因となっている遺伝子部分を編集するのではなく、ほかの遺伝子の発現調節に関与する部分(ノンコーディング領域)を編集することで糖尿病の発症とノンコーディング領域の関与を示唆した画期的な研究として注目されている。
以上、ここまでCRISPR/Cas9による糖尿病の研究をいくつか紹介した。ほかにもCRISPR/Cas9を用いた糖尿病患者のスクリーニング[17]など、ここに紹介した以上にさまざまなアプローチでゲノム編集の利用が検討されている。
ゲノム編集と糖尿病の未来
今回は誰もが耳にしたことがある糖尿病をテーマに、基礎的な知識の整理とゲノム編集の応用について紹介した。残念ながら、CRISPR/Cas9による糖尿病治療は研究途中であり、実際の臨床現場ではまだ利用されていない。しかし、すでにバイオファーマ業界で関心を集めており、2018年にはCRISPR Therapeutics社がViaCyte社と契約を結ぶなど、その動きは活発化している[18]。
糖尿病や肥満症などの疾患は、以前紹介したトランスサイレチンアミロイドーシスのような単一遺伝子疾患よりも複雑で治療が困難である[19]。しかし、CRISPR/Cas9のようなツールによって、その研究は確実に進歩している。ゲノム編集技術の応用に期待を抱きながら、今後もこうした研究に注目していきたい。
(文責:柴田潤一郎)
参照
[1] PRTIMES. “~約3人に1人がコロナ禍でお酒の頻度・量が増加~3人に1人が「お酒は飲めば強くなる」と誤解!飲み会再開に向けての不安、「行きたくない飲み会への参加」「アルハラ」など”
[2] 柴田潤一郎. 「CRISPR/Cas9で肥満症を改善!? ~ゲノム編集技術を用いたCommon diseasesの研究-①〜」
[4] Kao WH, Puddey IB, Boland LL, Watson RL, Brancati FL. Alcohol consumption and the risk of type 2 diabetes mellitus: atherosclerosis risk in communities study. Am J Epidemiol. 2001;154(8):748-757. doi:10.1093/aje/154.8.748
[5] Baliunas DO, Taylor BJ, Irving H, et al. Alcohol as a risk factor for type 2 diabetes: A systematic review and meta-analysis. Diabetes Care. 2009;32(11):2123-2132. doi:10.2337/dc09-0227
[7] NCBI. “Insulin.”
[8] MSDマニュアルプロフェッショナル. 「糖尿病(DM)」
[9] 日本糖尿病学会. 「糖尿病治療ガイド2016-2017」
[10] 国立研究開発法人国立成育医療研究センター. 「妊娠と妊娠糖尿病」
[11] 厚生労働省「令和元年国民健康・栄養調査」
[12] Hallakou-Bozec S, Vial G, Kergoat M, et al. Mechanism of action of Imeglimin: A novel therapeutic agent for type 2 diabetes. Diabetes Obes Metab. 2021;23(3):664-673. doi:10.1111/dom.14277
[13] 柴田潤一郎 「CRISPR/Cas9技術を応用したがん治療の未来 -ノーベル賞受賞技術の共演はあるのか-」
[14] Roh JI, Lee J, Park SU, et al. CRISPR-Cas9-mediated generation of obese and diabetic mouse models. Exp Anim. 2018;67(2):229-237. doi:10.1538/expanim.17-0123
[15] Maxwell KG, Augsornworawat P, Velazco-Cruz L, et al. Gene-edited human stem cell-derived β cells from a patient with monogenic diabetes reverse preexisting diabetes in mice. Sci Transl Med. 2020;12(540):eaax9106. doi:10.1126/scitranslmed.aax9106
[16] Bevacqua RJ, Dai X, Lam JY, et al. CRISPR-based genome editing in primary human pancreatic islet cells. Nat Commun. 2021;12(1):2397. Published 2021 Apr 23. doi:10.1038/s41467-021-22651-w
[17] Yi P, Morrow N. Applying CRISPR Screen in Diabetes Research. Diabetes. 2021;70(9):1962-1969. doi:10.2337/dbi20-0047
[18] FIERCE Biotech. Reversing diabetes with CRISPR and patient-derived stem cells
[19] 柴田潤一郎 「CRISPR/Cas9の静脈注射で夢の難病治療? ~ゲノム編集医療のこれまでとこれからを考える~」



